 |
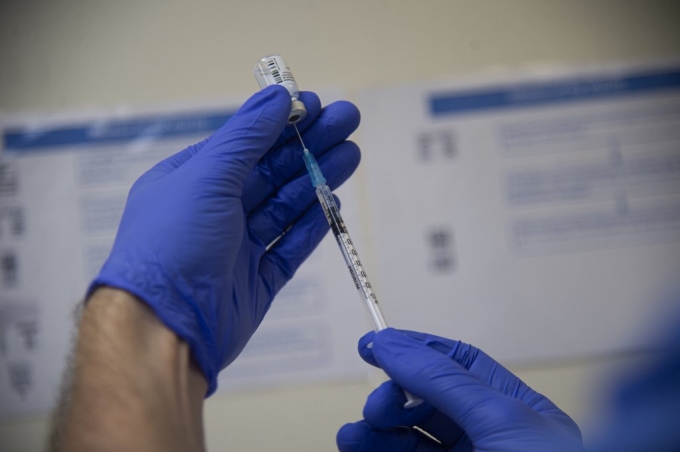
| /사진=AFP |
7일(현지시간) AFP통신, 뉴욕타임스(NYT) 등에 따르면 양사는 이날 성명을 통해 16세 이상 성인에 대한 코로나19 백신 사용을 정식 승인받기 위해 FDA에 효능과 안전성에 대한 자료를 포함한 임상 데이터를 제출했다고 밝혔다.
FDA에 코로나19 백신 정식 승인을 요청한 것은 화이자-바이오엔테크가 처음이다. 화이자-바이오엔테크 백신은 지난해 12월 말 FDA의 긴급사용 승인을 받았다. 이후 미국에 1억7000만회 분량의 백신을 공급했다.
긴급사용 승인은 코로나19 백신처럼 의료 현장에서 당장 사용해야 할 필요성이 클 때 내리는 일시적 조치로, 정식 승인 보다 절차가 상대적으로 까다롭지 않다. 화이자-바이오엔테크는 백신 정식 승인을 위해 FDA에 임상 3상에서의 2차 백신 투여 후 6개월까지의 자료 등 장기간의 후속 데이터를 제출할 예정이다.
앨버트 불라 화이자 최고경영자(CEO)는 성명에서 "미국 정부와 협력해 지난해 12월 이후 수백만명의 미국인에게 백신을 공급하면서 우리가 이뤄낸 엄청난 발전을 자랑스럽게 생각한다"며 "수개월 내 백신 정식 승인을 목표로 자료의 순차 제출(rolling submission)을 완료하고 검토를 지원할 수 있기를 기대한다"고 말했다.
FDA의 정식 승인에는 수개월이 소요될 것으로 예상되며, 정식 승인을 받을 경우 화이자-바이오엔테크는 시장에서 직접 백신을 판매할 수 있게 된다고 NYT는 설명했다.
화이자-바이오엔테크는 FDA에 12∼15세를 대상으로 한 코로나19 백신 긴급사용 승인도 요청한 상태다. FDA는 다음 주 초 승인 결정을 내릴 것으로 보인다.
한편 화이자-바이오엔테크에 이어 두 번째로 FDA의 긴급사용 승인을 받았던 모더나도 이달 중 FDA에 정식 승인을 신청할 예정이다.









![[더영상] '다치면 어쩌려고' 잔디밭서 낚시 연습…\](https://thumb.mt.co.kr/05/2024/04/2024041721160372364_1.jpg/dims/resize/201x/crop/201x130/optimize)
![어린이보호구역에 음주난동 골리앗…2초만에 제압한 다윗 경찰 [영상]](https://thumb.mt.co.kr/05/2024/04/2024041915333530747_1.jpg/dims/resize/201x/crop/201x130/optimize)





![광교도 아닌데…"수원 국평이 9억?" 외면받던 이 동네 '반전'[부릿지WALK]](https://thumb.mt.co.kr/11/2024/04/2024041816551096732_1.jpg/dims/resize/100x/optimize/)






![테슬라 압박하는 단 한 가지 문제…다음주 머스크가 답해야[오미주]](https://thumb.mt.co.kr/11/2024/04/2024041914093324262_1.jpg/dims/resize/100x/optimize/)



![일본 경제, 드디어 '정상' 되나 [PADO]](https://thumb.mt.co.kr/11/2024/04/2024041214300549771_1.jpg/dims/resize/100x/optimize/)



































![김수현X김지원, 애간장 녹이는 멜로..현빈♥손예진 넘나[★FOCUS]](https://menu.mt.co.kr/upload/main/2024/2024041816322057036482_mainTop.jpg)


!["광산 작업 가슴 아파서"…퇴역 항공기로 만든 전기차 배터리 케이스[월드콘]](https://thumb.mt.co.kr/06/2024/04/2024041915353043788_1.jpg)


























