 |
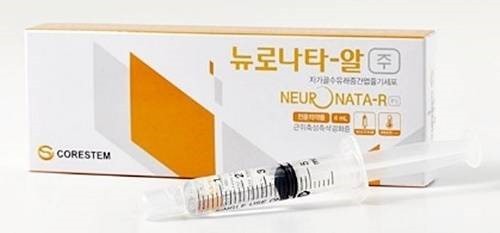
23일 업계에 따르면 지난 21일 기준 '뉴로나타-알주'의 임상3상 환자등록 비율이 52%를 기록했다.
코아스템 관계자는 "임상 환자등록이 예상보다 빠르게 진행되고 있다"면서 "임상3상의 완료 시점도 앞당겨 질 것으로 기대하고 있다"고 말했다.
코아스템은 지난 2월 115명 루게릭병 환자를 대상으로 5개 임상시험센터(한양대학교병원, 서울대학교병원, 고려대학교병원, 서울삼성병원, 양산부산대학교병원)에서 뉴로나타-알주의 임상3상을 시작했다. 이번 임상은 다기관, 무작위 배정, 이중맹검(이중눈가림), 위약 대조 방식으로 이뤄지며 각 환자들은 1년간 중 총 5회에 걸쳐 투여를 받게 된다.
안전성이 입증된 치료제를 비용 부담 없이 치료받을 수 있다는 점이 환자들의 임상 참여를 이끈 것으로 분석된다.
뉴로나타-알주는 루게릭병을 치료하기 위해 코아스템이 개발한 줄기세포치료제로, 2015년 식품의약품안전처로부터 임상3상을 조건으로 시판허가를 받았다.
회사 관계자는 "뉴로나타-알주가 이미 시장에서 판매되고 있는 치료제다 보니 약물 안전성에 대한 임상 환자들의 신뢰가 높다"고 설명했다.
루게릭 환자들의 치료제 선택이 넓지 않다는 점도 중요한 이유로 꼽힌다. 현재 허가받은 루게릭병 치료제는 코아스템의 뉴로나타-알주 외에 사노피의 '리루텍정(성분 리루졸, 1995년 허가)'과 미쓰비시타나베의 '라디컷주(성분 에다라본, 2015년 허가)'가 전부다. 특히 리루텍정과 라디컷주는 화학합성의약품이기 때문에 장기 복용할 경우 독성반응이 일어날 수 있다.
뉴로나타-알주 임상의 환자등록에 속도가 붙은 만큼 미국 식품의약국(FDA)의 허가 신청 시점도 앞당겨질 것으로 전망된다.
코아스템은 지난해 7월 FDA로부터 뉴로나타-알주의 임상3상을 승인받았다. 환자 수요가 높은 치료제인 만큼 국내 임상3상 결과로 FDA에 판매허가(BLA) 신청을 할 수 있도록 한 것.
코아스템 관계자는 "이번 임상은 2015년 판매 허가 당시 받았던 조건부 임상을 충족시키기 위해 진행됐지만, 모든 임상 설계 등은 미국 FDA 허가에 초점이 맞춰져 있다"고 말했다.
당초 회사 측은 최종 환자 투여를 2023년까지 마무리하고, 모든 데이터를 수집해 분석하는 과정을 거쳐, 2024년 FDA에 BLA를 신청한다는 계획이었다.
정희영 머니투데이방송 MTN 기자

















![[영상]북한 침투했던 그 무인기…표적 찍자, K9 포탄 140발 '쾅쾅'](https://thumb.mt.co.kr/11/2024/04/2024041717471540526_1.jpg/dims/resize/100x/optimize/)

![[단독]SK, 세종시에 반도체 공장 신설 추진](https://thumb.mt.co.kr/11/2024/04/2024041709093149706_1.jpg/dims/resize/100x/optimize/)





























!["학생 10명 거품 물고 쓰러져"…비극으로 끝난 '우정 여행'[뉴스속오늘]](https://thumb.mt.co.kr/10/2023/12/2023121717255330052_1.jpg/dims/resize/100x/optimize)




!["꼭 가야 해" 사람 가득 실은 배 30분 만에 침몰…292명 대참사[뉴스속오늘]](https://thumb.mt.co.kr/10/2023/10/2023100611053583558_1.jpg/dims/resize/100x/optimize)







































