 |
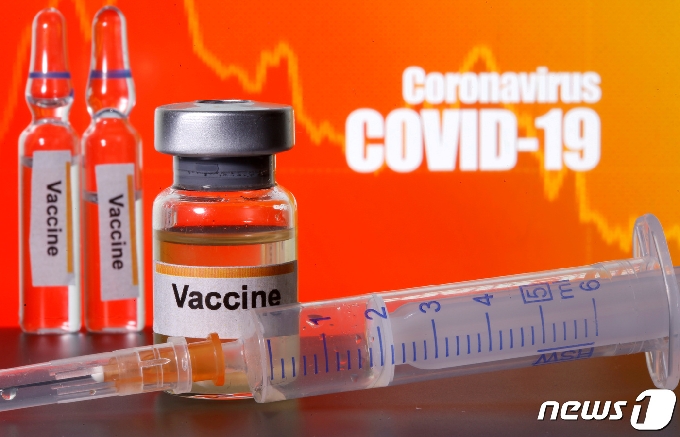
| 코로나19 백신 자료사진 ⓒ 로이터=뉴스1 |
13일(현지시간) 로이터통신에 따르면 이 기업들은 공동 개발한 백신 후보 'BNT162b1'과 'BNT162b2'가 FDA의 패스트트랙 지위를 얻었다고 밝혔다.
FDA의 패스트트랙 지위는 충족되지 않은 의료 수요를 해결하기 위해 신약과 백신에 대한 검토를 간소화하기 위해 부여된다.
앞서 바이오엔테크는 지난 1일 24명의 건강한 지원자들을 대상으로 백신 'BNT162b1'을 약 2회 투여한 후 28일이 지나자 감염자에게서 흔히 볼 수 있는 것보다 더 높은 수준의 항체가 생성됐다고 발표했다.
BNT162b1은 현재 미국과 독일에서 임상시험 중이며 초기 연구 결과가 이달 중 발표될 예정이다. 당국의 승인을 받을 경우 이르면 이달 말 최대 3만명이 참여하는 대규모 임상시험을 시작할 수 있을 것으로 보인다.
이 기업들은 현재 진행 중인 임상시험이 성공하고 백신 후보가 규제당국의 승인을 받을 경우 올해 말까지 최대 1억회, 2021년 말까지 12억회 분 이상의 백신을 생산할 수 있을 것으로 예상된다고 밝혔다.


























![모리스 창이 55세에 TSMC를 창업해 성공시킨 비결 [PADO]](https://thumb.mt.co.kr/11/2024/04/2024041914180910132_1.jpg/dims/resize/100x/optimize/)
!["8000원짜리 알리선 2000원"…중국 '직구' 외면할 수 있을까?[차이나는 중국]](https://thumb.mt.co.kr/11/2024/04/2024041817512119098_1.jpg/dims/resize/100x/optimize/)
![모디 인도 총리의 남부 지역 공략 [PADO]](https://thumb.mt.co.kr/11/2024/04/2024041914223276952_1.jpg/dims/resize/100x/optimize/)






















![[영상]"이강인, 손흥민에 패스 안 해 실점"…요르단전 이 장면 '시끌'](https://thumb.mt.co.kr/10/2024/02/2024021605405373481_1.jpg/dims/resize/100x/optimize)



![영하 13도, 길냥이 죽음 막을…'얼지 않는 물그릇'[남기자의 체헐리즘]](https://thumb.mt.co.kr/10/2024/01/2024012701364573421_1.jpg/dims/resize/100x/optimize)










![민희진 "주주간계약=모순 有"..하이브 "사실 아냐" 해명[★FOCUS]](https://menu.mt.co.kr/upload/main/2024/2024042621482692257147_mainTop.jpg)







![미국 대선, 6개주만 보면 답 나온다 [PADO 편집장의 '미국 대 미국']](https://i4.ytimg.com/vi/7kc1ddGnWtE/hqdefault.jpg)


















