 |
| (ПьЧб AFP=ДКНК1) ПьЕПИэ БтРк = 5РЯ(ЧіСіНУАЃ) СпБЙ ШФКЃРЬМК ПьЧбПЁ РжДТ ФкЗЮГЊ19 АЫЛчМвПЁМ СжЙЮРЬ ЧйЛъ АЫЛчИІ ЙоАэ РжДй. (C) AFP=ДКНК1 |
30РЯ ЙЬБЙ БЙИГКИАЧПј(NIH)РЬ ПюПЕЧЯДТ РгЛѓСЄКИ АјАГ ЛчРЬЦЎ ХЌИЎДЯФУЦЎЖѓРЬОѓНКПЁ ЕћИЃИщ СпБЙ ЙйРЬПРОїУМ ПСЛяЙйРЬПРАЁ ОЅРњПьПЁ КЛЛчИІ Еа ЖЧ ДйИЅ ЙйРЬПРЛч ОЦКИСЈАњ АГЙп СпРЮ ФкЗЮГЊ19 mRNA ЙщНХРЬ ЧіРч АГЙп ИЖСіИЗ ДмАшРЮ РгЛѓ 3ЛѓРЛ СјЧрСпРЮ АЭРИЗЮ ШЎРЮЕЦДй.
ЧиДч РгЛѓРК 18ММ РЬЛѓ 2ИИ8000ИэРЛ ДыЛѓРИЗЮ РЮЕЕГзНУОЦПЭ ИпНУФк 12АГ РЧЗсБтАќПЁМ СјЧр СпРЬДй. ПСЛяЙйРЬПРАЁ ХЌИЎДЯФУЦЎЖѓРЬОѓНКПЁ СІУтЧб ПЙЛѓ РгЛѓ ПЯЗсНУСЁРК ГЛГт 5ПљРЬДй.
ПУЧи 5ПљПЁДТ ЕПЗсЦђАЁИІ АХФЁБт Рќ ДмАшРЧ ГэЙЎЕЕ АјАГЕЦДй. РЬЙЬ ЛчЙщНХРЛ ХѕПЉЧб 300ИэПЁАд АГЙпСпРЮ mRNA ЙщНХРЛ УпАЁ СЂСОЧпРЛ ЖЇ СпШЧзУМ ОчРЬ НУГыЙщРЧ ФкЗЮГЊ ЙщНХРЛ УпАЁ СЂСОЧпРЛ ЖЇ КИДй 4Йш ГєДйДТ ГЛПыРЬ ГэЙЎПЁ НЧИА АЭРИЗЮ РќЧиСГДй. ХЌИЎДЯФУЦЎЖѓРЬОѓНКПЁ АјАГЕШ СЄКИ ЕюРИЗЮ ЙЬЗчОю КИИщ АГЙпРК НЧСІЗЮ ИЗЙйСі ДмАшПЁ СјРдЧб АЭРИЗЮ КИРЮДй.
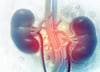
ЧиДч АГЙпРЛ ПСЛяЙйРЬПРПЭ АјЕПРИЗЮ СјЧрСпРЮ ОЦКИСЈРК ПРЙЬХЉЗа КЏРЬИІ АмГЩЧб КАЕЕРЧ mRNA ЙщНХ АГЙпПЁЕЕ ТјМіЧбДй. ОЦКИСЈРК РкЛч mRNA ЙщНХ ШФКИЙАСњ 'ABO1009-DP'РЧ ПРЙЬХЉЗа КЏРЬПЁ ДыЧб ОШРќМКАњ ШПДЩРЛ ЦђАЁЧЯДТ РгЛѓ 1/2ЛѓРЛ ПРДТ 8Пљ НУРлЧв АшШЙРЬДй. АњЧаРќЙЎСі ГзРЬУГПЁ ЕћИЃИщ ЧіРч СпБЙРК 6АГРЧ mRNA ЙщНХРЛ АГЙпСпРЮ АЭРИЗЮ РќЧиСГДй.
СпБЙРЬ СіГЧиБюСі РкУМ АГЙпЧб ЛчЙщНХ ШПДЩПЁ АЧб ШЎНХРЛ КИПДДйДТ СЁРЛ АЈОШЧЯИщ mRNA АшП ЙщНХ РгЛѓРЛ ЕПНУДйЙпРћРИЗЮ СјЧрЧЯДТ ЧіРч АГЙп ЕПЧтРК РЬЗЪРћРЬДй.
СпБЙРЬ СіБнБюСі ЧуАЁЧб ЙщНХ 7СОРК И№ЕЮ ЛчЙщНХРЬДй. РЬ АЁПюЕЅ НУГыЦЪАњ НУГыЙщРЬ ДыЧЅ ЙщНХРЬДй. НУГыЦЪ ЙщНХРК СпБЙ БЙПЕСІОрЛчРЮ СпБЙРЧОрБзЗь ЛъЧЯ 'СпБЙЛ§ЙА'ПЁМ АГЙпЧпДй. НУГыЙщ ЙщНХРК 'КЃРЬТЁАњШяЛ§ЙАСІЧА'РЬЖѕ ШИЛчПЁМ ГЛГѕРК ЙщНХРЬДй. НУГыЦЪАњ НУГыЙщ ЙщНХРК mRNA ЙцНФРЧ ШРЬРк, И№ДѕГЊ ЙщНХРЬГЊ ЙйРЬЗЏНККЄХЭЙцНФРЧ ОЦНКЦЎЖѓСІГзФЋ, ОсМО ЙщНХАњ ДоИЎ 'Лч(он)ЙщНХ(killed vaccine)' ЙцНФРИЗЮ АГЙпЕЦДй. КДПјБеРЛ ПРЬГЊ ШЧаРћРЮ ЙцЙ§РИЗЮ КёШАМКШНУХВ ЧќХТРЧ ЙщНХРЮЕЅ КёБГРћ ОШРќЧЯСіИИ ИщПЊЗТРК ЖГОюСіДТ АЭРИЗЮ ОЫЗССГДй.
НУГыЦЪАњ НУГыЙщРК ЕЈХИКЏРЬАЁ ШЎЛъЕЧДј СіГЧи 7Пљ РќШФИІ БтСЁРИЗЮ БЙСІРћРИЗЮ 'ЙАЙщНХ' ГэЖѕПЁ НУДоЗШДй. ИљАёАњ ФЅЗЙ, ЙйЗЙРЮ ЕюПЁМ ЧиДч ЙщНХРЧ ГєРК СЂСОЗќПЁЕЕ КвБИЧЯАэ ШЎСјРкЕщРЬ РЬЗЪРћРИЗЮ КвОюГЕАэ ХТБЙРК НУГыЙщ МіРдРЛ СпДмЧЯАэ mRNA ЙщНХРЛ ЕЕРдЧпДй. ДчНУ РгЛѓНУЧш АсАњИІ ХфДыЗЮ НУГыЙщРЬ ЙрШљ ФкЗЮГЊ19 ПЙЙц ШПАњДТ 50.4%ЗЮ ММАшКИАЧБтБИ(WHO) УжМв БЧАэ БтСиРЮ 50%ИІ АЁБюНКЗЮ ГбАхДй. ПЙЙцШПАњ 90%ИІ ГбОюМБ ШРЬРкПЭ И№ДѕГЊ Ею mRNA ЙщНХ РгЛѓ АсАњПЭ ТїРЬАЁ ЧіАнЧпДй.
ЧЯСіИИ, СпБЙРК РкБЙ ЙщНХРЬ ШПДЩРЬ ОјДйДТ СіРћПЁ АЧЯАд ЙнЙпЧпДй. СіГЧи 7Пљ 22РЯ РкПРИЎСЈ СпБЙ ПмБГКЮ ДыКЏРЮРК ДчНУ ЙАЙщНХ ГэЖѕ АќЗУ, КъИЎЧЮРЛ ХыЧи "СЁСЁ ИЙРК АњЧаРћЁЄРЬМКРћ ИёМвИЎАЁ СпБЙ ЙщНХПЁ ОШРќЧЯДйДТ ЖѓКЇРЛ КйРЬАэ РжДй"Ич "РЬАЭРК СпБЙ ЙщНХРЬ ШПАњРћРЬАэ ОШРќЧЯДйДТ АЭРЛ УцКаШї МГИэЧбДй"Аэ ЙрЧћДй. "ИЙРК БЙАЁРЧ СжПф РЮЛчЕщРЬ СпБЙ ЙщНХРЬ ЧіСі ЙцПЊПЁ ФПДйЖѕ БтПЉИІ ЧпДйАэ ЦђАЁЧЯАэ РжРИИч СпБЙ ЙщНХРЛ СЂСОЧб ПмБЙ БЙЙЮЕЕ ТљМКЧЅИІ ДјСіАэ РжДй"АэЕЕ АСЖЧпДй.
РЬРЬ ААРК ЙАЙщНХ ГэЖѕ ШФ 1ГтПЉАЃ mRNA ЙщНХ АГЙпПЁ ГЊМ ЧіРч РгЛѓ ИЗЙйСі ДмАшПЁ РЬИЅ МРРЬДй. ГзРЬУГДТ mRNA ЙщНХРЧ СпБЙ УжСО НТРЮ ПЉКЮДТ ЧіРч СјЧрСпРЮ РгЛѓ 3Лѓ АсАњПЁ ЕћЖѓ СТПьЕЩ АЭРИЗЮ КИРЮДйАэ КаМЎЧпДй. РкУМ АГЙпЧб mRNA ЙщНХРЬ ЛчЙщНХКИДй ШПАњАЁ ГєДйДТ СЁРЬ ШЎРЮЕХ РЧЗсЧіРхПЁ ХѕРдЕЩ АцПь, ШЎСјРк ЙпЛ§СіПЊРЛ КРМтЧЯДТ СпБЙРЧ 'СІЗЮ ФкЗЮГЊ' СЄУЅПЁЕЕ КЏШАЁ ПУСіЕЕ АќАЧРЬДй.

















![ЕЙПЌ ЛчЖѓСј 70Ды РчЗТАЁЁІГЛПЌГр С§ НУИрЦЎ КЮНЅДѕДЯ НУНХРИЗЮ[ДКНКМгПРДУ]](https://thumb.mt.co.kr/11/2024/04/2024042417433499310_1.jpg/dims/resize/100x/optimize/)






























!["ЧаЛ§ 10Иэ АХЧА ЙААэ ОВЗЏСЎ"ЁІКёБиРИЗЮ ГЁГ 'ПьСЄ ПЉЧр'[ДКНКМгПРДУ]](https://thumb.mt.co.kr/10/2023/12/2023121717255330052_1.jpg/dims/resize/100x/optimize)
![[ПЕЛѓ]"РЬАРЮ, МеШяЙЮПЁ ЦаНК ОШ Чи НЧСЁ"ЁІПфИЃДмРќ РЬ РхИщ 'НУВј'](https://thumb.mt.co.kr/10/2024/02/2024021605405373481_1.jpg/dims/resize/100x/optimize)

!["ВР АЁОп Чи" ЛчЖї АЁЕц НЧРК Йш 30Ка ИИПЁ ФЇИєЁІ292Иэ ДыТќЛч[ДКНКМгПРДУ]](https://thumb.mt.co.kr/10/2023/10/2023100611053583558_1.jpg/dims/resize/100x/optimize)





!["ДКСјНК КМИ№ЗЮ ЧљЙк" ЧЯРЬКъ, ЙЮШёСј 12АЁСі СжРхПЁ ЙнЙк [АјНФ][РќЙЎ]](https://menu.mt.co.kr/upload/main/2024/2024042616282322557637_mainTop.jpg)














![ЙЬБЙ ДыМБ, 6АГСжИИ КИИщ Дф ГЊПТДй [PADO ЦэС§РхРЧ 'ЙЬБЙ Ды ЙЬБЙ']](https://i4.ytimg.com/vi/7kc1ddGnWtE/hqdefault.jpg)


















